Enthalpie - Entropie
| Unbedingt sehenswert . . . |
Betrachten wir einen Motorkolben im Arbeitstakt und ohne Zündung, diesmal ohne die Verbindung zur Kurbelwelle. Er wird also bei geschlossenen
Ventilen von OT nach UT geschoben von der Luft, die er vorher verdichtet hat. Eigentlich könnte er sogar noch weiter, wäre der Zylinder nur
unbegrenzt lang.
|
Dieses Phänomen hat Atkinson für seine Erfindung
ausgenutzt. |
Zum Stillstand käme er, Reibung einmal vernachlässigt, wenn der Druck im Brennraum gleich dem Umgebungsdruck wäre. Nur unter diesen
Bedingungen könnte man die geleistete Arbeit einigermaßen exakt bestimmen, die man hier Volumenänderungsarbeit nennt.
Arbeit ist als Kraft mal Weg (W = F • s) definiert. Und da sich der Druck als Kraft durch (gedrückte Kolbenober-) Fläche ergibt, lässt sich die Arbeit
jetzt als Fläche mal Weg mal Druck (W = A • s • p) berechnen. Der Kolbenweg mal seiner Oberfläche ergibt einen Zylinder V. Also lässt sich die
Volumenänderungsarbeit als die Volumenänderung mal dem Druck (W = ΔV • p) bestimmen.
Ein schöner Begriff 'Volumenänderungsarbeit' und auch leicht einsehbar, da man sich klar das gegen den Atmosphärendruck hinzugewonnene
Volumen vorstellen kann. Betrachtet man den Brennraum als zum System gehörig mit der verschiebbaren Kolbenoberfläche als eine der
Systemgrenzen, dann ist von der dem System innewohnenden Energie ein Teil für die Änderung dieser Systemgrenze verwandt worden.
Eigentlich wird die innere Energie als Enthalpie H bezeichnet. Allerdings kann man sie so nicht bestimmen, sondern immer nur ihre Änderung. Und
die wird hier durch die Volumenänderung erreicht. So ist die Enthalpie die Summe aus innerer Energie und Volumenänderungsarbeit (H = U + p • V).
So und jetzt stellen Sie sich bitte vor, diese Kolbenbewegung wäre unendlich langsam verlaufen. Es hätte also keine Druckerhöhung (isobare
Zustandsänderung) stattgefunden, weil diese in Wärme umgewandelt und an die Umgebung abgegeben worden wäre. Der Prozess wäre sogar
umkehrbar (reversibel), weil auch die Temperaturabsenkung bei sinkendem Druck durch die Umgebung ausgeglichen worden wäre.
| Enthalpie ist eine Energieform, SI-Einheit
Joule (J) |
Prozesse ohne Druckänderung sind sehr häufig. Überall, wo kein Deckel drauf ist, also keine geschlossenen Räume vorhanden sind, kommen sie vor,
z.B. beim (Stahl-)Schmelzen. Es gibt sie auch in geschlossenen Räumen. So verläuft ein großer Teil des Arbeitstaktes beim ersten Dieselmotor von
1897 unverändert mit dem Verdichtungsenddruck von gut 30 bar.
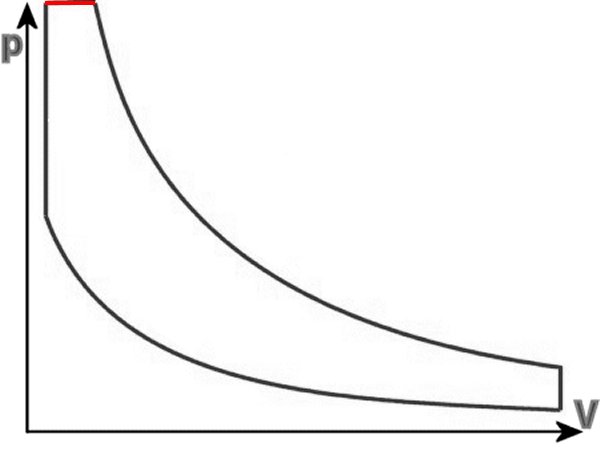
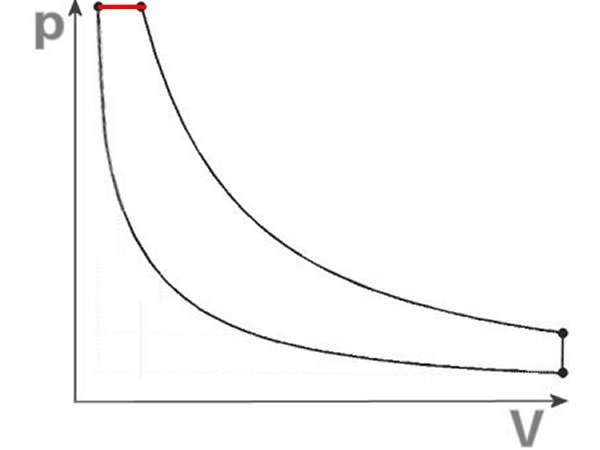
Hier zwei idealisierte pV-Diagramme, berechenbare Kurvenverläufe, die den wirklichen Verlauf möglichst gut nachempfinden sollen. Oben mit vier
Kurven, unten der Seiliger-Prozess mit fünf. Obwohl er besser angepasst ist, enthält er doch noch ein
Stück (rot gekennzeichneter) isobaren
Kurvenverlaufs.
Man stellt sich vor, dass der Verbrennungsdruck sich am Anfang so langsam entwickelt, dass er von der Volumenänderung durch den nach UT
gehenden Kolben aufgefangen wird. Deshalb wird der Dieselmotor bisweilen noch als Gleichdruckmotor bezeichnet, der Ottomotor wegen seiner
durch elektrische Zündung und anderen Kraftstoff als Gleichraummotor.
Also kann bei dem oben beschriebenen, sehr langsam ablaufenden Prozess die Enthalpie-Differenz als die nach außen übertragene Wärme
angesehen werden. Vielleicht nicht ganz, weil natürlich durch die Volumenänderung eine andere Verteilung (Ordnung) erzeugt wird, auch wenn die
besonders langsam erfolgt.
| Entropie S in Enthalpie durch absolute Temperatur (J/K) |
Und genau das berücksichtigt die oben im Video sehr anschaulich erklärte Entropie, die z.B. hier bei den (idealen) Gasen eine größere Bedeutung
hat, weil deren Position und Ordnung im Raum millionenfach verschieden sein kann. Die genaue Erfassung von Energieströmen beim Betrieb
thermodynamischer Systeme ist nicht nur zur Erfassung des Wirkungsgrads von großer Bedeutung.
Maßnahmen zur Ersparnis von Brennstoff sind allerdings mindestens 200 Jahre alt. Schon die Erfindung der Dampfmaschine durch James Watt (1736
- 1819) war eigentlich die Verbesserung der Erfindung von Thomas Newcomen. Ottos Viertaktmotor war die u.a. energetische Verbesserung der
Lenoir-Maschine von 1860 und der Dieselmotor hat wiederum die Dampfmaschine ersetzt.
Und was hat die Entropie mit der Temperatur zu tun? Die Bewegung der Moleküle steigt bei Gasen mit der Temperatur. Das verringert die Ordnung
und erhöht somit die Entropie. Damit sind wir beim 2. Hauptsatz der Thermodynamik angelangt, wonach jede freiwillig ablaufende Zustandsänderung die
Entropie vergrößert. 02/17
|