Entalpía - Entropía
Considere un pistón del motor en el ciclo de trabajo y sin ignición, esta vez sin la conexión al cigüeńal. Por lo tanto, se empuja con las válvulas cerradas desde el punto muerto superior hasta el punto muerto inferior
del aire, que que él previamente ha comprimido. En realidad, podría ir aún más lejos, si el cilindro solo fuera indefinidamente largo.
| Este fenómeno ha sido explotado por Atkinson para su invención. |
Se detendría, la fricción sería ignorada, si la presión en la cámara de combustión es igual a la presión ambiental. Solo bajo estas condiciones podría determinar el trabajo realizado con cierta precisión, lo que se
denomina trabajo de cambio de volumen.
El trabajo se define como la fuerza multiplicado con la ruta (W = F • s). Y allí la presión resultados como fuerza dividida por área (superficie del pistón presionado), el trabajo ahora se puede calcular como el
área multiplicada por el ruta multiplicado por la presión (W = A • p). La ruta del pistón multiplicado con su superficie da un cilindro V. Por lo tanto, el trabajo de cambio de volumen se puede determinar como el
cambio de volumen multiplicado por la presión ((W = ΔV • p).
Un buen término 'trabajo de cambio de volumen' y también fácil de entender, porque se puede imaginar claramente el volumen ganado contra la presión atmosférica. Considerando que la cámara de combustión
pertenece al sistema con la superficie del pistón desplazable como uno de los límites del sistema, entonces ha sido utilizado de la energía inherente del sistema una parte para cambiar este límite del sistema.
En realidad, la energía interna se llama entalpía H. Sin embargo, no puedes determinarlos de esa manera pero siempre solo su cambio. Y esto se logra aquí mediante el cambio de volumen. Entonces la entalpia es
la suma de la energía interna y el trabajo de cambio de volumen (H = U + p • V).
Así que ahora imagina que este movimiento del pistón habría sido infinitamente lento. Así no habría habido un aumento de la presión (cambio de estado isobárico) porque se habría convertido en calor y se habría
liberado al medio ambiente. El proceso sería incluso reversible, porque la reducción de temperatura se habría compensado con una presión decreciente a través del medio ambiente.
| La entalpía es una forma de energía, unidad SI Joule (J) |
Los procesos sin cambio de presión son muy comunes. Dondequiera que no haya una tapa, y no hay espacios cerrados, se ocurrir, por ejemplo, durante la fundición (de acero). También están disponibles en
espacios cerrados. Por lo tanto, una gran parte de la ciclo de trabajo en el primer motor diesel desde 1897 se ejecuta sin cambios con la presión final de compresión de más de 30 bar.
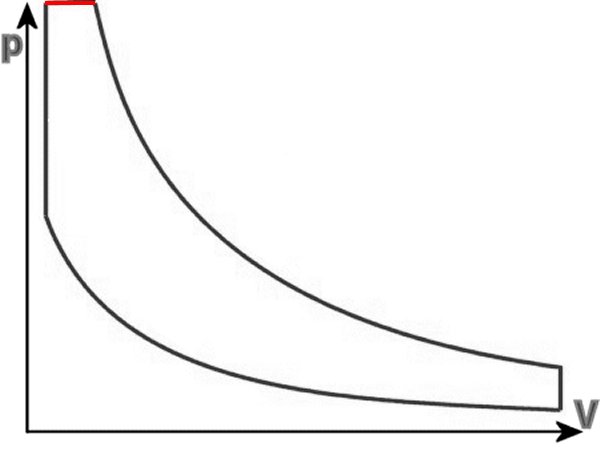
Aquí hay dos diagramas pV idealizados, curvas calculables, que deben simular el curso real lo mejor posible. Arriba con cuatro curvas, debajo del proceso Seiliger con cinco. Aunque está mejor adaptado, todavía contiene una pieza de curva isobara (marcada en rojo).
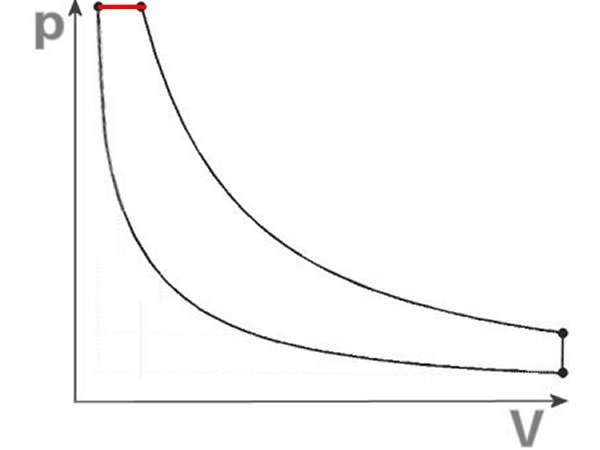
Se imagina que la presión de combustión se desarrolla inicialmente tan lentamente que queda atrapada por el cambio de volumen cuando el pistón va al punto muerto inferior. Por lo tanto, el motor diesel a veces se
conoce como un motor de presión constante, el motor de gasolina debido a su encendido eléctrico y otro combustible como un motor de volumen constante.
Por lo tanto, en el proceso muy lento descrito anteriormente, la diferencia de entalpía puede considerarse como el calor transmitido al exterior. Tal vez no del todo, porque por supuesto, el cambio de volumen, se
genera una distribución diferente (orden), incluso si eso ocurre especialmente lento.
| Entropía S en entalpía debido a la temperatura absoluta (J/K) |
Y eso es exactamente lo que toma en cuenta la entropía, que es más importante para los gases (ideales) porque su posición y orden en el espacio puede ser un millón de veces diferente. La detección precisa de los
flujos de energía en el funcionamiento de los sistemas termodinámicos no solo es de gran importancia para la detección de rendimiento de energía.
Sin embargo, las medidas para ahorrar combustible tienen al menos 200 ańos de antigüedad. Incluso la invención de la máquina de vapor por James Watt (1736 - 1819) fue en realidad la mejora de la invención por
Thomas Newcomen. El motor de cuatro tiempos de Otto fue, entre otras cosas, la mejora energética de la máquina Lenoir de 1860 y el motor diesel reemplazó a su vez la máquina de vapor.
żY qué tiene que ver la entropía con la temperatura? El movimiento de las moléculas aumenta en los gases con la temperatura. Esto reduce el orden y así aumenta la entropía. Esto nos lleva a la segunda ley de la
termodinámica, según el cual cualquier cambio voluntario de estado aumenta la entropía. 02/17
|