 Tabla periµdica 2 Tabla periµdica 2

Los 118 elementos estÃn dispuestos en un orden particular. Los cortos quÚmicos se utilizan por razones de espacio, aquÚ se omiten los nombres de los elementos. Y para acostumbrarse a las abreviaturas
quÚmicas y por
razones de espacio, se omiten aquÚ los nombres completos de los elementos. Por cierto, estos no se basan en el idioma inglÕs (ferrum - hierro) sino en el latÚn.
Los nºmeros ordinales son llamativos, indican un orden. Ese es el nºmero de cargas, los protones en el nºcleo atµmico y los electrones en la capa atµmica. El nºmero de neutrones aºn no se considera aquÚ.
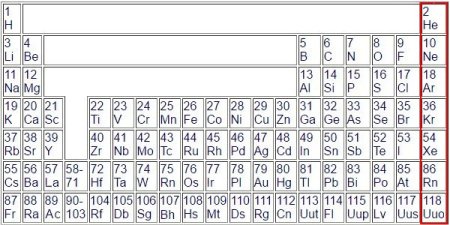
La brecha en la parte superior en el medio se debe al hecho de que los elementos de los ocho grupos principales deben agruparse, 1 y 2 en el extremo izquierdo y 3 al 8 en el extremo derecho. En el medio los
subgrupos,
por cierto todos los metales. En la parte inferior izquierda de los grupos laterales hay marcadores de posiciµn. Los nºmeros atµmicos del 58 al 71 son para los isµtopos de Lanthan (Lathanides) y del 90 al 103
para los isµtopos de Actinium (Actinoides).
El sistema tiene su nombre de los perÚodos, que son las lÚneas. En el capÚtulo Electrones, aprendiµ que existen nºmeros cuÃnticos principales para diferenciar los grupos de electrones del 1 al 7. Por lo tanto,
con los dos elementos hidrµgeno y helio, solo hay un grupo principal en el primer perÚodo no completamente ocupado. Esto aumenta hasta los siete grupos principales presentes en la sÕptima lÚnea (perÚodo).
Los electrones recogidos en el ºltimo nºmero cuÃntico principal estÃn todos en el lado exterior de la capa atµmica, tambiÕn llamados 'electrones de valencia'. Sus nºmeros son muy importantes para las
reacciones con otros Ãtomos, ya que la ºnica forma de intercambiar electrones es aquÚ, pero solo si no se alcanza el nºmero mÃximo posible. El nºmero de electrones de valencia determina la pertenencia a un
grupo principal particular, con la excepciµn del helio.
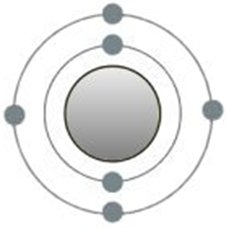
El Ãtomo de carbono carece de cuatro electrones de valencia, por lo que puede, por ejemplo, vincular cuatro Ãtomos de hidrµgeno con un solo electrµn en la capa mÃs externa. Por lo tanto, se hace referencia al carbono
como tetravalente y al hidrµgeno como monovalente. De los Ãtomos de oxÚgeno, solo hay dos al carbono, como ya sugiere el nombre diµxido de carbono.
La formaciµn de dicha molÕcula suele ser el resultado de una reacciµn. Se dice que el carbono y el oxÚgeno reaccionan entre sÚ, lo que en una ecuaciµn de reacciµn para la formaciµn de agua se ve asÚ, por ejemplo:
2 H2 + O2 -> 2 H2O
¢Por quÕ hay el '2' respectivamente delante de la 'H' y la 'H2O'? Porque siempre necesitas dos Ãtomos de hidrµgeno y solo un Ãtomo de oxÚgeno, lo cual ocurre naturalmente como una molÕcula de dos
Ãtomos. Porque siempre necesitas dos Ãtomos de hidrµgeno y solo un Ãtomo de oxÚgeno, lo cual ocurre en la naturaleza como una molÕcula de dos Ãtomos.
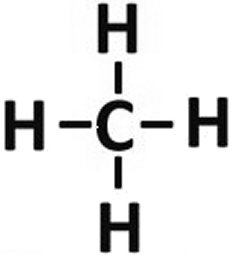
AquÚ se representan grÃficamente las respectivas letras iniciales del nombre latino del hidrocarburo y entremedio las lÚneas para el nºmero de enlaces. Las lÚneas tambiÕn pueden ser mºltiples y el carbono tambiÕn
puede combinarse consigo mismo, formando asÚ una cadena, como ocurre en el combustible diesel, por ejemplo.

| Es comºn en quÚmica que ciertos compuestos se abandonen debido a otros compuestos mÃs
deseables. |
|