 Periodensystem 2 Periodensystem 2

Hier die 118 Elemente in einer bestimmten Ordnung. Und damit man sich an die chemischen Kurzzeichen gewöhnt und aus Platzgründen, sind hier die ausgeschriebenen Namen der Elemente
weggelassen. Die basieren übrigens nicht auf der englischen Sprache, sondern sind lateinischen Ursprungs (Ferrum - Eisen).
Auffallend sind natürlich die Ordnungszahlen, die hier eine Reihenfolge vorgeben. Es ist die Anzahl der Ladungen, also der Protonen im Atomkern und gleichzeitig der Elektronen in der Atomhülle. Die
Anzahl der Neutronen ist hier noch nicht berücksichtigt.
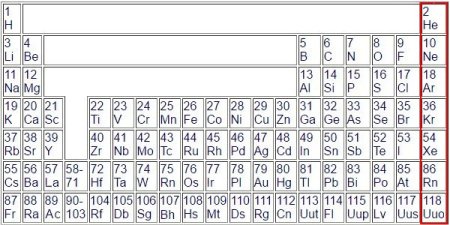
Die Lücke oben in der Mitte entsteht, weil man die Elemente der acht Hauptgruppen zusammenfassen will, 1 und 2 ganz links und 3 bis 8 ganz rechts. Zu den Nebengruppen gehören die in der Mitte,
übrigens alles Metalle. Links unten bei den Nebengruppen gibt es Platzhalter. Die Ordnungszahlen von 58 bis 71 stehen für die Isotope von Lanthan (Lanthanoiden) und die von 90 bis 103 für die Isotope von
Actinium (Actinoiden).
Seinen Namen hat das System von den Perioden, das sind die Zeilen. Im Kapitel über Elektronen erfahren Sie, dass es Hauptquantenzahlen zur Unterscheidung von Elektronengruppen von 1 bis 7 gibt.
Also gibt es bei den beiden Elementen Wasserstoff und Helium in der nicht vollständig besetzten ersten Periode nur eine Hauptgruppe. Das steigert sich bis zu den sieben vorhandenen Hauptgruppen in
der siebten Zeile (Periode).
Die in der jeweils letzten Hauptquantenzahl erfassten Elektronen sind ganz außen in der Atomhülle, auch 'Valenzelektronen' genannt. Deren Zahl ist für Reaktionen mit anderen Atomen sehr wichtig, weil
es nur hier zum regen Austausch von Elektronen kommen kann, allerdings nur, wenn die maximal mögliche Zahl nicht erreicht wird. Die Anzahl der Valenzelektronen bestimmt die Zugehörigkeit zu einer
bestimmten Hauptgruppe mit Ausnahme von Helium.
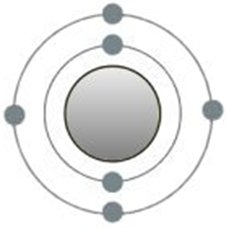
Dem Kohlenstoff-Atom fehlen so vier Valenzelektronen, weshalb es z.B. vier Wasserstoffatome mit nur einem Elektron auf der äußersten Schale an sich binden kann. Man bezeichnet daher Kohlenstoff als
vierwertig und Wasserstoff als einwertig. Von den Sauerstoffatomen sind es nur zwei am Kohlenstoff, wie der Name Kohlendioxid schon verrät.
Die Bildung eines solchen Moleküls ist in der Regel das Ergebnis einer Reaktion. Man sagt, Kohlenstoff und Sauerstoff reagieren miteinander, was in einer Reaktionsgleichung zur Bildung von Wasser z.B. so
aussieht:
2 H2 + O2 -> 2 H2O
Wozu es die '2' jeweils vor dem 'H' und dem ' H2O' gibt? Weil man eben immer zwei Atome Wasserstoff und nur ein Atom Sauerstoff braucht, der aber in der Natur als Molekül zweier Atome
vorkommt. Man erzeugt also zwei Moleküle, was auf der rechten Seite der Reaktionsgleichung deutlich wird. Diese Anzahl kommt dann vor die komplette Molekülbezeichnung.
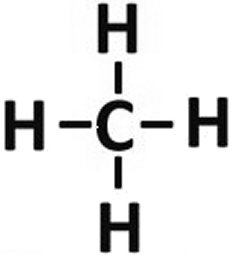
Grafisch dargestellt ergeben sich hier für den Kohlenwasserstoff die jeweiligen Anfangsbuchstaben der lateinischen Bezeichnung und dazwischen die Striche für die Anzahl der Bindungen. Die Striche können
auch mehrfach sein und der Kohlenstoff kann sich auch mit sich selbst verbinden, dadurch eine Kette bilden, wie sie z.B. im Dieselkraftstoff vorkommt.
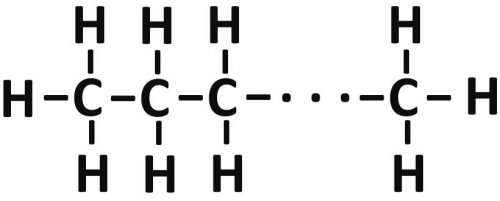
| Es kommt in der Chemie häufig vor, dass bestimmte Verbindungen wegen anderer,
wünschenswerterer aufgegeben werden. |
|