 Metalle 2 Metalle 2

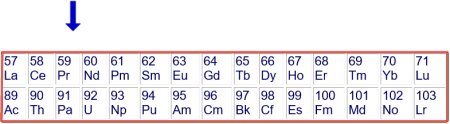
Wie Sie oben sehen, gehören die allermeisten Elemente zu den Metallen es ist die mit Abstand größte Gruppe. Hinzuzählen muss man noch die Elemente mit Ordnungszahlen 58-71 und 90-103 darunter.
Es sind fast ausnahmslos Stoffe, die sich durch hohe Festigkeit auszeichnen. Trotzdem sind sie bleibend verformbar, und können so verdichtet werden, dass ihre Streckgrenze und damit auch ihre
Festigkeit noch gesteigert wird.
Bei der Reihenfolge der Tabelle wurden schon früh die Eigenschaften der verschiedenen Elemente berücksichtigt. Und zwar so gut, dass später entdeckte sich nahtlos einordnen ließen. Vielleicht kann man
das am besten an den Metallen erklären, die ca. 70 Prozent der Elemente ausmachen. Glänzend und formbar sind sie wohl alle, aber manche reagieren besonders heftig mit Wasser. Die sind z.B. hier in
der linken Spalte angeordnet.
In der Mitte sind die Metalle mit weniger drastischen Reaktionen aufgeführt. Die ihnen nachgesagte Wärme- und besonders die elektrische Leitfähigkeit nimmt nach rechts hin ab. Die Bezeichnung stammt
eigentlich eher von der Wirkung zwischen den Atomen, den die Leitfähigkeit bedingenden freien Fluss der Elektronen. Die Bezeichnung 'Metall' kennzeichnet also die Art der Bindung.
| Elektronen bestimmen die Eigenschaften eines Stoffes. |
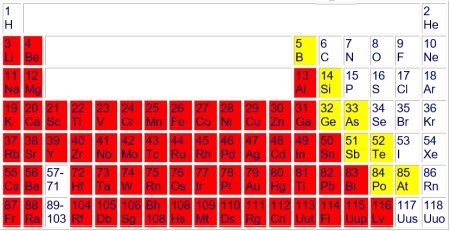
Einige Metalle besitzen neben ihrer elektrischen Leitfähigkeit auch magnetische Eigenschaften. Hier haben wir farblich abgesetzt noch ein paar Elemente, die nicht so ganz als Metalle gelten. Man
bezeichnet sie als Halbleiter. Ihre Bedeutung ist in den letzten 50 Jahren enorm gestiegen.
| Leichtestes Metall | Lithium | 0,53 g/cm3 |
| Schwerstes Metall | Osmium | 22,5 g/cm3 |
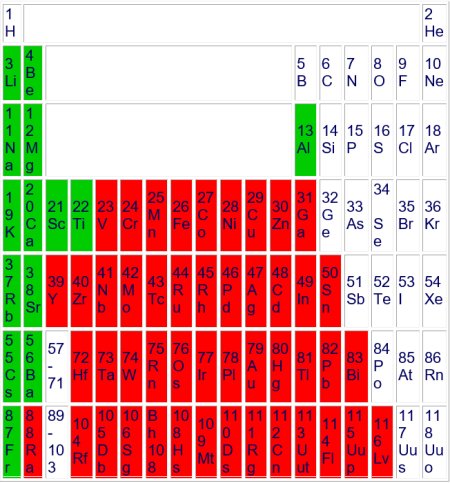
Hier sind die Leichtmetalle hervorgehoben. So werden alle Metalle mit einer Dichte von weniger als 5 kg/dm3 oder 5 g/cm3 bezeichnet. Interessant, dass das mit 4,5 g/cm3
schwerste Leichtmetall Titan
schon fast im Mittelblock angeordnet ist.
|