|
|
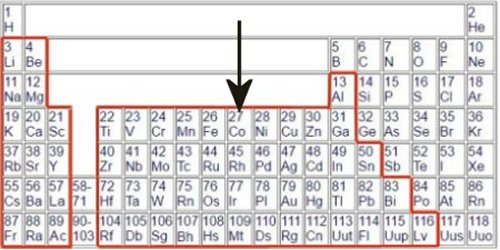
 Cobalt Cobalt
Immer wieder sehen sich Besitzer/innen von reinen Elektroautos Vorw■rfen ausgesetzt, dass ihre Autos so umweltfreundlich nicht seien. Nun gut, die Argumente, die sich auf den aktuellen Strommix
beziehen, lassen sich mit der Vision von 100 Prozent erneuerbarer Energie entkrðften. Aber was hat es mit den offensichtlichen Problemen bei der Herstellung von Elektroautos auf sich?
Die Motoren sind wohl auf dem Weg zur Besserung, wenn man ■berhaupt diesen Term benutzen darf. Aber was ist mit den Batterien? Hier ist neben Lithium ein Stoff gefragt, der einen groÔen Produzenten
hat, die 'Demokratische Republik' Kongo mit ■ber 50 Prozent. Das ist doppelt so viel wie der zweistðrkste f—rdert. Das macht abhðngig und sollte vermieden werden. So soll Tesla immerhin mit der dritten
Batterie-Generation des Model 3 deutlich mehr als die Hðlfe des Metalls Cobalt eingespart haben.
Zusammen mit seinem chemischen Kurzzeichen schreiben wir hier eher 'Cobalt' statt 'Kobald'. Der Name ist nicht zufðllig dem eines Kobolds ðhnlich, sondern von ihm abgeleitet, weil man dieses Metall
fr■her beim Abbau f■r Silber gehalten hat, was aber nicht dessen Eigenschaften hatte. Man konnte schlicht nichts mit ihm anfangen und nannte es das Produkt von 'Kobolden', weil es wie Silber aussah, aber
keines war. Stattdessen wurden beim Versuch des Erschmelzens giftige Arsendðmpfe Gase frei.
Der mangelnde Nutzen hat sich z.B. mit der Anwendung als Blau-Fðrbemittel f■r Glas und Keramik geðndert. 1780 wurde es als chemisches Element anerkannt und seit Anfang des 20. Jahrhunderts ist es
auch anderweitig n■tzlich, z.B. als Bestandteil in besonders harten Legierungen, f■r die Naturheilkunde und f■r die inzwischen fast v—llig verschwundenen Farbfernseher. Heutzutage ist das
Anwendungsgebiet 'Batterien' das eindeutig gr—Ôte, wobei die E-Autos noch einen relativ kleinen Anteil haben. Cobalt ist in seinen Eigenschaften seinen beiden Nachbarn im Periodensystem sehr ðhnlich,
Eisen und Nickel, so magnetisierbar wie Eisen, grau gefðrbt, mit der Dichte von Kupfer.
Cobalt kann sogar eine h—here magnetische Anziehungskraft entwickeln als Eisen und ist schwerer oxidierbar. Die Vorw■rfe wollen auch deshalb nicht verstummen, weil Cobalt so schlecht zu gewinnen ist.
Es kommt in den entsprechenden Erzen nur mit Anteilen von weit unter einem Prozent vor. Lange war es nur eine Beif■gung der Gewinnung von Kupfer und Nickel. Allerdings ist angesichts der erzielbaren
Preise aus dem einstigen Neben- ein Hauptprodukt geworden. Und klar muss auch sein, dass der Bedarf mit dem Anteil der Batterien von E-Autos noch deutlich steigen kann.
Wozu nutzt man eigentlich Cobalt? Wir konzentrieren uns auf die Batterien. Fast alle enthalten Cobalt. Das Gros teilt sich auf in jeweils Lithium und Nickel mit mehrheitlich Magnesium und Cobalt oder
Cobalt und Aluminium. Letztere gelten als die leistungsfðhigeren und werden z.B. von Tesla verwendet, werden aber auch f■r nicht ganz so sicher wie die anderen gehalten. In der jetzigen Diskussion verweisen die
Tesla-Fans darauf, dass es dieser amerikanischen Firma verboten ist, Rohstoffe wie Cobalt aus bestimmten, politisch instabilen Lðndern zu beziehen, wie in diesem Beispiel dem Kongo.
GroÔe Firmen betreiben die Minen dort, aber knapp 20 Prozent werden auch privat von Familien z.T. deren Kindern gewonnen, insgesamt ■ber 100.000 Menschen, oft illegal und mit sehr unfalltrðchtigen Hilfsmitteln.
Nat■rlich k—nnen diese die gewonnenen Erze nicht raffinieren, sondern verkaufen an Zwischenhðndler. Es ist also m—glich, dass so gewonnenes Cobalt gleichsam unkontrolliert auf den Weltmarkt gelangt. VW
verweist auf die Responsible Raw Materials Initiative und deren Zertifizierungsssystem f■r Cobaltschmelzen, um die Herkunft des Materials f■r seine Batterien nachweisen zu k—nnen.
AuÔerdem ist der Konzern Mitglied der Global Battery Alliance des Weltwirtschaftsforums, der die soziale und —kologische Nachhaltigkeit in der Wertsch—pfungskette von Batterierohstoffen sicherstellen soll nicht nur
von Cobalt.
Schlimm wird die Diskussion, wenn es um Zahlen geht. So wird z.B. in USA behauptet, es seien noch 4,5 g Cobalt im Model 3 statt 11 g im ersten Model S. Allerdings gibt man nicht die jeweilige Batteriekapazitðt an.
Ein deutsche Tesla-Fan sagt, es seinen 2,8 Prozent. Beim Audi e-tron soll das Batteriegewicht laut Hersteller 700 kg betragen. Das Model 3 mit kleinstem Akku kðme dann umgerechnet auf 400 kg. Davon 2,8 Prozent
wðren ■ber 11 kg. Sie sehen, selbst die Tesla-Fans sind sich untereinander nicht einig. In der VW-ID.3-Batterie sollen nach deren Aussage sogar '■ber 12 Prozent' Cobalt bzw. 'vier Mal mehr Cobalt als im Tesla'
enthalten sein, wobei wieder nicht gesagt wird, welcher Akku aus dem ID.3 denn gemeint ist. Mit den Zahlen sollten die entsprechenden youtuber etwas vorsichtiger umgehen.
Viel wichtiger ist aber die Frage, wozu Cobalt an der Kathode einer Lithium-Ionen Batterie gebraucht wird. Dazu muss man dort von in der Gesamtheit elektrisch neutralem Co-Ni-Mg mit Sauerstoff und Lithium-Ionen
und an der Anode von ebenfalls ungeladenem Graphit ausgehen. Wird die Batterie geladen, verlassen Elektronen der Metalloxide via Kabel diesen Block in Richtung Anode und hinterlassen dort insgesamt positive
Ladung. Daraufhin wandern die Lithium-Ionen durch den Separator direkt zum Graphit und lagern sich dort zusammen mit den ankommenden Elektronen an. Kathode und Anode sind wieder elektrisch ausgeglichen.
Beim Entladen kehrt sich der Prozess um. Die Ausgangssituation ist, dass Lithium-Atome auf der Anodenseite in einem kristallinen Graphitverbund sind, ohne mit diesem durch irgendeine chemische Reaktion
verbunden zu sein. Beim Entladen der Batterie entweicht wieder das jeweilige Elektron von der ðuÔersten Schale des Lithium-Atoms. Dieses wird wieder zum positiv geladenen Teilchen, einem Lithium-Ion. Die
Lithium-Ionen im Graphitkristall werden von der verbliebenen Co-Ni-Mg-Verbindung mit Sauerstoff der Kathode angezogen, k—nnen wieder durch den Separator ungehindert hindurch und finden eine Stelle zum
Einlagern. Es entsteht wieder die das potentialfreie Metalloxid mit den Lithium-Ionen. Bei VW besteht der Metallteil aus Nickel- und Mangansulfat, aber auch hier mit Cobaltsulfat. Je reiner deren Mischung und auch des
wasserfreien elektrolytischen Transportmittels zwischen Kathode und Anode, desto langlebiger und besser funktionierend die Batterie.
Das Metalloxid bildet also keineswegs nur den Aufbewahrungsort f■r die Lithium-Ionen, sondern spielt mit seinen Elektronen auch im (Ent-) Ladungsprozess eine Rolle. Und offensichtlich ist die Anwesenheit von
Cobalt hierbei wichtig f■r die Energiedichte der Kathode. Es ist offensichtlich f■r eine groÔe Leistungsfðhigkeit der Batterie wohl zur Zeit noch unersetzbar. Der Senior Vice President bei BASF, einem der gr—Ôten
Hersteller von Kathodenmaterial, sagt, dass man die 124.000 Tonnen insgesamt pro Jahr bei 30 Millionen Autos mit 90 kWh-Akku selbst bei den gr—Ôtm—glichen Einsparungen auf mehr als das Dreifache steigern
m■sse.
| Deutsche Untertitel m—glich . . . |
|
|